Tóm tắt Luận án Nghiên cứu tổng hợp vật liệu mới trong cấy ghép và tái tạo xương trên cơ sở hydrogel composite sinh học gồm biphasic calcium phosphate và polymer sinh học (gelatin, chitosan)

Trang 1

Trang 2

Trang 3

Trang 4

Trang 5

Trang 6

Trang 7

Trang 8

Trang 9
Trang 10
Tải về để xem bản đầy đủ
Bạn đang xem 10 trang mẫu của tài liệu "Tóm tắt Luận án Nghiên cứu tổng hợp vật liệu mới trong cấy ghép và tái tạo xương trên cơ sở hydrogel composite sinh học gồm biphasic calcium phosphate và polymer sinh học (gelatin, chitosan)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Tóm tắt Luận án Nghiên cứu tổng hợp vật liệu mới trong cấy ghép và tái tạo xương trên cơ sở hydrogel composite sinh học gồm biphasic calcium phosphate và polymer sinh học (gelatin, chitosan)

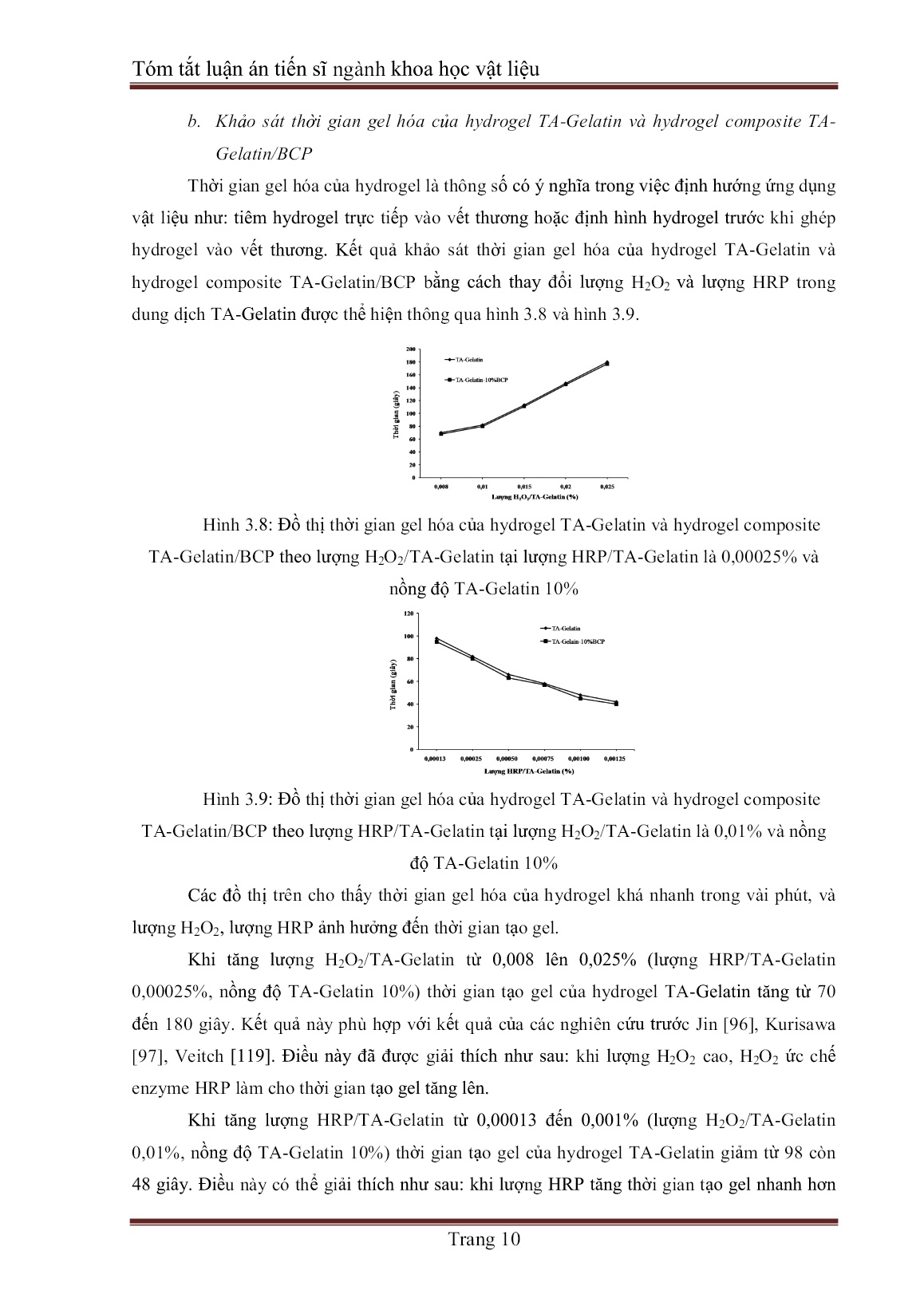
qua phản ứng giữa nhóm amin của tyramin và nhóm carboxyl của gelatin. Phổ 1H NMR của TA-Gelatin đƣợc đo trong H2O Hình 3.7: Phổ 1H NMR của TA-Gelatin Phổ cộng hƣởng từ hạt nhân có các tín hiệu của các proton có trong gelatin nhƣ pic đơn ở vị trí 4,8 ppm (proton vị trí anomeric carbone của gelatin) và các pic ở vị trí 0,8- 4,6ppm (proton của các nhóm alkyl của gelatin. Kết quả này phù hợp với các nghiên cứu của Park [116, 117]. Sự xuất hiện của pic đôi ở vị trí 6,754; 7,105 ppm trong phổ cộng hƣởng từ hạt nhân của TA-Gelatin chứng tỏ sự có mặt của proton Ha, Hb (nhóm -CH=CH- trong nhân thơm) của tyramin. Kết quả này phù hợp với các nghiên cứu của Park [116, 117], điều này chứng tỏ TA- Gelatin đã đƣợc tổng hợp thành công. b. Xác định lượng TA trong TA-Gelatin Lƣợng TA trong TA-Gelatin đƣợc xác định bằng phổ tử ngoại – khả kiến (UV-Vis). Kết quả phân tích lƣợng TA trong TA-Gelatin cho thấy trong 100mg TA-Gelatin có 0,538mg TA tƣơng đƣơng 0,00392 mmol TA. 3.2.2. Tổng hợp hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP a. Xác định lượng H2O2 tối thiểu để tạo gel Theo nghiên cứu của Kurisawa [97] số mol H2O2 tối thiểu cần phản ứng là 60% số mol TA. Trên cơ sở đó, chúng tôi tính lƣợng H2O2 tối thiểu cần phản ứng với TA trong 10mg TA-Gelatin để tạo gel là 0,00235 mmol tƣơng đƣơng lƣợng H2O2 là 0,008% trong dung dịch TA-Gelatin 10%. Ngoài ra nồng độ H2O2 không sử dụng cao hơn 0,25% vì sẽ gây độc đối với tế bào [119]. Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 10 b. Khảo sát thời gian gel hóa của hydrogel TA-Gelatin và hydrogel composite TA- Gelatin/BCP Thời gian gel hóa của hydrogel là thông số có ý nghĩa trong việc định hƣớng ứng dụng vật liệu nhƣ: tiêm hydrogel trực tiếp vào vết thƣơng hoặc định hình hydrogel trƣớc khi ghép hydrogel vào vết thƣơng. Kết quả khảo sát thời gian gel hóa của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP bằng cách thay đổi lƣợng H2O2 và lƣợng HRP trong dung dịch TA-Gelatin đƣợc thể hiện thông qua hình 3.8 và hình 3.9. Hình 3.8: Đồ thị thời gian gel hóa của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP theo lƣợng H2O2/TA-Gelatin tại lƣợng HRP/TA-Gelatin là 0,00025% và nồng độ TA-Gelatin 10% Hình 3.9: Đồ thị thời gian gel hóa của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP theo lƣợng HRP/TA-Gelatin tại lƣợng H2O2/TA-Gelatin là 0,01% và nồng độ TA-Gelatin 10% Các đồ thị trên cho thấy thời gian gel hóa của hydrogel khá nhanh trong vài phút, và lƣợng H2O2, lƣợng HRP ảnh hƣởng đến thời gian tạo gel. Khi tăng lƣợng H2O2/TA-Gelatin từ 0,008 lên 0,025% (lƣợng HRP/TA-Gelatin 0,00025%, nồng độ TA-Gelatin 10%) thời gian tạo gel của hydrogel TA-Gelatin tăng từ 70 đến 180 giây. Kết quả này phù hợp với kết quả của các nghiên cứu trƣớc Jin [96], Kurisawa [97], Veitch [119]. Điều này đã đƣợc giải thích nhƣ sau: khi lƣợng H2O2 cao, H2O2 ức chế enzyme HRP làm cho thời gian tạo gel tăng lên. Khi tăng lƣợng HRP/TA-Gelatin từ 0,00013 đến 0,001% (lƣợng H2O2/TA-Gelatin 0,01%, nồng độ TA-Gelatin 10%) thời gian tạo gel của hydrogel TA-Gelatin giảm từ 98 còn 48 giây. Điều này có thể giải thích nhƣ sau: khi lƣợng HRP tăng thời gian tạo gel nhanh hơn Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 11 do lƣợng enzyme xúc tác nhiều hơn nên liên kết ngang tạo thành nhanh hơn dẫn đến rút ngắn thời gian tạo gel [96]. Trong trƣờng hợp hydrogel composite TA-Gelatin/BCP thời gian tạo gel ít thay đổi so với thời gian tạo gel của hydrogel TA-Gelatin. Ví dụ: thời gian tạo gel của TA-Gelatin là 70 giây khi nồng độ TA-Gelatin 10%, lƣợng HRP/TA-Gelatin 0,00025 % và lƣợng H2O2/TA- Gelatin 0,008%, khi có thêm BCP với lƣợng 10% thời gian tạo gel là 68 giây. Điều này có thể giải thích do tƣơng tác của các hạt BCP và gelatin. Nhóm chức NH2, OH, COOH của gelatin liên kết hydrogen với nhóm OH của HAp trong BCP, ngoài ra còn có liên kết tạo phức của nhóm NH2 của gelatin và ion Ca 2+ của BCP [120-123]. Các liên kết giữa các hạt BCP và gelatin làm mật độ liên kết của hydrogel composite tăng do đó thời gian tạo gel của hydrogel composite giảm. Trái lại, BCP làm tăng độ nhớt của dung dịch nên ảnh hƣởng đến quá trình khuếch tán xúc tác dẫn đến thời gian tạo liên kết ngang tăng dần. Dẫn đến kết quả thời gian tạo gel của hydrogel composite TA-Gelatin/BCP ít thay đổi so với thời gian tạo gel của hydrogel TA-Gelatin. Tóm lại: thời gian gel hóa có thể điều chỉnh cho phù hợp với nhu cầu thực tiễn ứng dụng bằng cách thay đổi lƣợng H2O2 hoặc HRP trong dung dịch TA-Gelatin. 3.2.3. Khảo sát hình thái của hydrogel TA-Gelatin và hydrogel composite TA- Gelatin/BCP Hình 3.10: Hình ảnh SEM của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP với các lƣợng BCP khác nhau Hình ảnh SEM đƣợc sử dụng để khảo sát hình thái học của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP với các lƣợng BCP khác nhau (hình 3.10). Kết quả cho thấy hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP có cấu trúc không gian ba chiều xốp. Trong khi vật liệu đƣợc tổng hợp bằng phƣơng pháp đúc không có cấu trúc xốp nhƣ hydrogel [124-127]. Cấu trúc không gian 3 chiều, xốp của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP tạo khoảng cƣ trú cho tế bào dịch chuyển và lƣu thông các yếu tố chuyển hóa tạo xƣơng. Ngoài ra, tế bào và mạch máu có thể phát triển bên trong các lỗ xốp của vật liệu giúp xƣơng phát triển bên trong vật liệu [27, 123]. Do đó, cấu trúc xốp của hydrogel và hydrogel composite phù hợp cho ứng dụng trong lĩnh vực cấy ghép và tái tạo xƣơng. Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 12 3.2.6. Khảo sát khối lƣợng suy giảm sinh học của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP Phƣơng pháp phân tích trọng lƣợng theo thời gian đƣợc sử dụng để khảo sát khối lƣợng suy giảm của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/ BCP, kết quả đƣợc thể hiện qua hình 3.11. Hình 3.11: Đồ thị khối lƣợng (%) suy giảm của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP theo thời gian Kết quả khảo sát khối lƣợng suy giảm của hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP cho thấy hydrogel không có BCP khối lƣợng suy giảm nhanh hơn nhiều so với hydrogel composite có BCP. Lƣợng BCP trong hydrogel composite càng tăng thì khối lƣợng (%) suy giảm của hydrogel composite càng nhỏ. Ví dụ: sau 18 giờ TA-Gelatin suy giảm 97% và TA-Gelatin-5%BCP suy giảm 66%, TA-Gelatin-10%BCP suy giảm 45%. Điều này có thể giải thích do tƣơng tác của các hạt BCP và gelatin. Nhóm chức NH2, OH, COOH của gelatin liên kết hydrogen với nhóm OH của HAp trong BCP, ngoài ra còn có liên kết tạo phức của nhóm NH2 của gelatin và ion Ca 2+ của BCP [120-123]. Tuy vậy, khối lƣợng suy giảm gần 100% sau 42 giờ không phù hợp để ứng dụng trong lĩnh vực cấy ghép và tái tạo xƣơng. 3.3. HYDROGEL COMPOSITE TA-PEG-GELATIN/BCP 3.3.1. Tổng hợp TA-PEG-Gelatin a. Xác định thành phần, cấu trúc của TA-PEG-Gelatin Tổng hợp NPC PEG NPC Để tổng hợp TA-PEG-Gelatin cần phải hoạt hóa hai nhóm OH cuối của PEG bởi p nitrophenyl chloroformate tạo sản phẩm trung gian NPC-PEG- NPC. Phổ 1H NMR đo trong dung môi H2O Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 13 Hình 3.13: Phổ 1H NMR của NPC PEG NPC Phổ cộng hƣởng từ hạt nhân có các tín hiệu của các proton có trong PEG nhƣ pic đơn ở δ = 3,64ppm chứng tỏ sự có mặt của proton H trên mạch PEG ở vị trí liên kết với nhóm (-O- CH2-CH2-).Tín hiệu pic ở δ = 4,42ppm là tín hiệu của proton H trên mạch PEG liên kết với nhóm NPC (NPC-O-CH2-). Hai tín hiệu pic ở δ = 7,38ppm và δ = 8,26ppm là tín hiệu của proton H của nhóm NPC (-CH=CH-). Các kết quả này phù hợp với nghiên cứu của Park [117]. Mức độ hoạt hóa đạt khoảng 97% đƣợc tính từ tỷ lệ tích phân của proton thơm (NPC) và proton methylene (PEG). Tổng hợp TA PEG NPC Trong giai đoạn này, liên kết urethane đƣợc tạo thành từ phản ứng giữa nguyên tử nitơ trong phân tử tyramin và nhóm C=O của hợp chất NPC-PEG-NPC tạo sản phẩm TA-PEG- NPC. Phổ 1H NMR đo trong dung môi H2O Hình 3.15: Phổ 1H NMR của TA PEG NPC Phổ cộng hƣởng từ hạt nhân có các tín hiệu của các proton thơm của nhóm Tyramin ở δ= 6,77 và 7,02 ppm. Ngoài ra, ở vùng 8,29 – 8,38 ppm thể hiện tín hiệu của proton thơm (NPC). Kết quả này phù hợp với nghiên cứu của Park [171]. Khoảng 67% NPC đƣợc thay thế bởi TA thu đƣợc từ kết quả tính tỷ lệ tích phân của proton thơm (NPC) và proton thơm liên hợp của TA. Tổng hợp TA-PEG-Gelatin Trong giai đoạn phản ứng này, phản ứng urethane đƣợc tạo thành từ nhóm NH2 trên mạch gelatin và nhóm C=O của sản phẩm trung gian NPC PEG TA. Phổ 1H NMR đo trong dung môi H2O Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 14 Hình 3.17: Phổ 1H NMR TA-PEG-Gelatin Phổ cộng hƣởng từ hạt nhân có các tín hiệu của các proton có trong gelatin nhƣ mũi đơn ở vị trí 4,8 ppm (proton vị trí anomeric carbone của gelatin) và các mũi ở vị trí 0,8- 4,6ppm (proton của các nhóm alkyl) của gelatin. Pic đơn ở δ = 3,64ppm là tín hiệu nhóm methylene của mạch PEG. Hai tín hiệu pic ở δ = 6,77ppm và δ = 7,09ppm là tín hiệu proton liên hợp vòng thơm của tyramin. Kết quả này phù hợp với các nghiên cứu của Park [116,117]. Phổ đồ FTIR của gelatin [phụ lục 8] có những pic 1636 và 1550 cm-1 đặc trƣng cho dao động N-H của amin, các pic này không xuất hiện trong phổ đổ FTIR của TA-PEG-gelatin [phụ lục 9] do phản ứng urethane đƣợc tạo thành từ nhóm NH2 trên mạch gelatin và nhóm C=O của sản phẩm trung gian NPC PEG TA khi tổng hợp TA-PEG-gelatin. b. Xác định lượng TA trong TA-PEG-Gelatin Lƣợng TA trong TA-PEG-Gelatin đƣợc xác định bằng phổ tử ngoại-khả kiến (UV- Vis). Kết quả phân tích lƣợng TA trong TA-PEG-Gelatin cho thấy trong 100mg TA-PEG- Gelatin có 0,83904mg TA tƣơng đƣơng 0,00612mmol TA. 3.2.2. Tổng hợp hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG- Gelatin /BCP a. Xác định lượng H2O2 tối thiểu để tạo gel Theo nghiên cứu của Kurisawa [97] số mol H2O2 tối thiểu cần phản ứng là 60% số mol TA. Trên cơ sở đó, chúng tôi tính lƣợng H2O2 tối thiểu cần phản ứng với TA trong 100mg TA-PEG-Gelatin để tạo gel là 0,00367 mmol tƣơng đƣơng lƣợng H2O2 là 0,0125% trong dung dịch TA-PEG-Gelatin 10%. Ngoài ra nồng độ H2O2 không sử dụng cao hơn 0,25% vì sẽ gây độc đối với tế bào [119]. b. Khảo sát thời gian gel hóa của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP Kết quả khảo sát thời gian gel hóa của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP bằng cách thay đổi lƣợng H2O2 và lƣợng HRP trong dung dịch TA-PEG-Gelatin đƣợc thể hiện thông qua hình 3.18 và hình 3.19. Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 15 Hình 3.18: Đồ thị thời gian gel hóa của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP theo lƣợng H2O2/TA-Gelatin tại lƣợng HRP/TA-Gelatin là 0,00025% và nồng độ TA-PEG-Gelatin 10% Hình 3.19: Đồ thị thời gian gel hóa của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP theo lƣợng HRP/TA-PEG-Gelatin là 0,0125% và nồng độ TA-PEG-Gelatin 10% Các đồ thị trên cho thấy thời gian gel hóa của hydrogel khá nhanh trong vài phút, và lƣợng H2O2, lƣợng HRP ảnh hƣởng đến thời gian tạo gel. Khi tăng lƣợng H2O2/TA-PEG-Gelatin từ 0,0125 lên 0,1% (lƣợng HRP/TA-PEG- Gelatin 0,0025%, nồng độ TA-PEG-Gelatin 10%) thời gian tạo gel của hydrogel TA-PEG- Gelatin tăng từ 50 đến 168 giây. Khi tăng lƣợng HRP/TA-PEG-Gelatin từ 0,00013 đến 0,01 % (lƣợng H2O2/ TA-PEG- Gelatin 0,0125%, nồng độ TA-PEG-Gelatin 10%) thời gian tạo gel của hydrogel TA-PEG- Gelatin giảm từ 80 còn 77 giây. Trong trƣờng hợp hydrogel composite TA-PEG-Gelatin/BCP thời gian tạo gel ít thay đổi so với thời gian tạo gel của hydrogel TA-PEG-Gelatin. Ví dụ: thời gian tạo gel của TA- PEG-Gelatin là 80 giây khi nồng độ TA-PEG-Gelatin 10%, lƣợng HRP/TA-PEG-Gelatin 0,0013% và lƣợng H2O2/TA-PEG-Gelatin 0,0125%; khi có thêm BCP với lƣợng 10% thời gian tạo gel là 77 giây. Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 16 3.3.3. Khảo sát hình thái hydrogel TA-PEG-Gelatin và hydrogel composite TA- PEG-Gelatin/BCP Hình 3.20: Hình ảnh SEM của hydrogel TA-PEG-Gelatin và hydrogel composite TA- PEG-Gelatin/BCP với các lƣợng BCP khác nhau Hình ảnh SEM đƣợc sử dụng để khảo sát hình thái học của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP với các lƣợng BCP khác nhau (hình 3.20). Kết quả cho thấy hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP có cấu trúc không gian ba chiều xốp phù hợp cho ứng dụng trong lĩnh vực cấy ghép và tái tạo xƣơng. 3.3.4. Khảo sát khối lƣợng suy giảm sinh học của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP Hình 3.21: Đồ thị % khối lƣợng suy giảm của TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP theo thời gian Kết quả khảo sát khối lƣợng suy giảm của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP cho thấy hydrogel không có BCP khối lƣợng suy giảm nhanh hơn so với hydrogel composite có BCP. Lƣợng BCP trong hydrogel composite càng tăng thì khối lƣợng (%) suy giảm của hydrogel composite càng nhỏ. Ví dụ: sau 3 tuần TA- PEG-Gelatin suy giảm 12% và TA-PEG-Gelatin-5%BCP suy giảm 11%, TA-PEG-Gelatin - 10%BCP suy giảm 10%. Hydrogel composite TA-PEG-Gelatin, TA-PEG-Gelatin 5%BCP và TA-PEG-Gelatin- 10%BCP hydrogel composite có khối lƣợng mất đi sau 4 tuần là 20,89; 19,49 và 17,73%. Hydrogel TA-PEG-Gelatin có thời gian suy giảm dài hơn hydrogel TA-Gelatin. Thời gian suy giảm của hydrogel composite TA-PEG-Gelatin/BCP và hydrogel TA-PEG-Gelatin dài hơn 4 tuần, điều này khẳng định PEG gắn lên mạch polymer gelatin làm gelatin khó suy giảm. Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 17 Tóm lại, hydrogel TA-Gelatin và hydrogel composite TA-Gelatin/BCP suy giảm gần 100% sau 42 giờ nhƣng sau khi biến tính gắn PEG vào gelatin thì khối lƣợng suy giảm chậm lại rõ rệt, sau 4 tuần hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin chỉ suy giảm gần 20% khối lƣợng. 3.3.5. Đánh giá tính tƣơng hợp sinh học của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP Tính tƣơng hợp sinh học của hydrogel composite TA-PEG-Gelatin/BCP đƣợc khảo sát trên cơ sở độc tính tế bào của vật liệu và trên cơ sở sự bám dính và phát triển của tế bào trên vật liệu. a. Tính tương hợp sinh học của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP trên cơ sở độc tính tế bào Hình 3.22: Đồ thị khảo sát độc tính tế bào của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP Độc tính tế bào của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG- Gelatin/BCP đƣợc khảo sát bằng phƣơng pháp MTT trên tế bào xƣơng MG-63. Kết quả khảo sát tính tƣơng hợp sinh học trên cơ sở độc tính tế bào của hydrogel TA- PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP cho thấy: với các nồng độ pha loãng dung dịch chiết mẫu khác nhau (0, 25, 50, 75, 100%) cả hydrogel TA-PEG-Gelatin lẫn hydrogel composite TA-PEG-Gelatin/BCP đều có tỉ lệ sống của tế bào trên 97%. Dựa trên tiêu chuẩn ISO 10993-5, 1999 (vật liệu không độc đối với tế bào khi tại các nồng độ pha loãng dung dịch chiết mẫu tỉ lệ tế bào sống đều cao hơn 70%), cho thấy hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP đều không độc đối với tế bào. Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 18 b. Tính tương hợp sinh học của hdrogel TA-PEG-Gelatin và hydrogel composite TA- PEG-Gelatin/BCP trên cơ sở sự bám dính và phát triển của tế bào trên vật liệu Hình 3.23: Sự bám dính và phát triển của tế bào xƣơng MG-63 trên hydrogel TA-PEG- Gelatin và hydrogel composite TA-PEG-Gelatin/BCP sau thời gian 5 ngày Khảo sát sự bám dính và phát triển của tế bào xƣơng MG-63 trên hydrogel TA-PEG- Gelatin và hydrogel composite TA-PEG-Gelatin/BCP đƣợc quan sát dƣới kính hiển vi huỳnh quang. Nhân tế bào màu xanh sau khi nhuộm tế bào với thuốc nhuộm DAPI. Kết quả (hình 3.23) cho thấy: sau 5 ngày, tế bào bám và phát triển rất tốt thành 1 lớp phủ trên bề mặt cả hydrogel và hydrogel composite. Do đó có thể khẳng định tính tƣơng hợp sinh học cao của hydrogel TA-PEG-Gelatin và cả hydrogel composite TA-PEG-Gelatin/BCP đối với tế bào xƣơng MG-63. Điều này có thể giải thích bởi gelatin và BCP đều có khả năng kích thích, thúc đẩy sự phát triển của tế bào, đặc biệt BCP thúc đẩy quá trình phát triển của tế bào xƣơng do BCP có khả năng hấp thụ protein của môi trƣờng nuôi cấy trong quá trình phát triển tế bào xƣơng[139-144]. Mặt khác các hạt BCP tạo tạo bề mặt gồ ghề giúp tế bào bám dính tốt [145, 146]. Kết quả thu đƣợc cho thấy hydrogel TA-PEG-Gelatin và hydrogel composite TA- PEG-Gelatin/BCP có nhiều tiềm năng ứng dụng trong tái tạo mô xƣơng. 3.3.6. Khảo sát khả năng tạo khoáng của hydrogel TA-PEG-Gelatin và hydrogel composite TA-PEG-Gelatin/BCP Hình 3.24: Hình ảnh SEM và EDS của hydrogel TA-PEG-Gelatin sau 2 tuần ngâm trong dung dịch SBF Khả năng tạo khoáng đƣợc sử dụng để dự đoán các hoạt tính sinh học của vật liệu trong nghiên cứu in vitro, in vivo chẳng hạn nhƣ khả năng tạo mầm và phát triển tinh thể apatite carbonate trên bề mặt của vật liệu [121,122]. Chúng tôi khảo sát sự hình thành khoáng apatite carbonate của hydrogel TA-PEG- Gelatin sau thời gian ngâm vật liệu 2 tuần trong dung dịch SBF và đƣợc đông khô. Quan sát hình ảnh SEM (hình 3.24) với kích thƣớc 100µm ta thấy hydrogel TA-PEG-Gelatin vẫn giữ Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 19 đƣợc thành phần, cấu trúc xốp. Hình ảnh SEM với kích thƣớc 10µm cho thấy trên bề mặt hydrogel xuất hiện các tinh thể lớn 1-2µm. Kết quả phân tích EDS các tinh thể đó (hình 3.24) cho thấy xuất hiện các nguyên tố Na (36,69%), Cl (50,91%) của muối NaCl trong dung dịch SBF và xuất hiện nguyên tố Au (12,40%) do lớp vàng phủ lên mẫu để phân tích EDS. Hình 3.25: Hình ảnh SEM và EDS của hydrogel composite TA-PEG-Gelatin/BCP sau 2 tuần ngâm trong dung dịch SBF Bảng 3.4: Thành phần % khối lƣợng các nguyên tố trong phân tích EDS của hydrogel composite TA-PEG-Gelatin/BCP sau 2 tuần ngâm trong dung dịch SBF Mẫu nghiên cứu % khối lƣợng C O Na P Cl Ca TA-PEG-Gelatin-5%BCP 17,38 28,54 3,45 11,67 5,67 33,30 TA-PEG-Gelatin-10%BCP 10,45 24,17 2,53 13,11 2,95 46,79 Khảo sát bằng hình ảnh SEM hydrogel composite TA-PEG-Gelatin/BCP với lƣợng BCP 5% và 10%, sau thời gian ngâm vật liệu 2 tuần trong dung dịch SBF và đƣợc đông khô. Kết quả cho thấy hydrogel composite TA-PEG-Gelatin/BCP vẫn giữ đƣợc cấu trúc xốp. Hình ảnh SEM với kích thƣớc 3µm (hình 3.25) cho thấy trên bề mặt hydrogel composite xuất hiện các hạt tinh thể rất nhỏ. Phân tích EDS các hạt tinh thể trên (hình 3.25) cho thấy ngoài các nguyên tố Na, Cl còn xuất hiện nguyên tố C, O, P, Ca là các nguyên tố cấu thành calcium phosphate, calcium carbonate. Kết quả phân tích trong bảng 3.4 cho thấy phần lớn mầm tinh thể chứa các nguyên tố Ca, P, O, C là nguyên tố cấu thành calcium phosphate và calcium carbonate và phần còn lại là các tinh thể chứa nguyên tố Na, Cl. Các kết quả nghiên cứu của Mohamed [123], Amir [124], Gu [125] khẳng định: BCP tăng cƣờng khả năng tạo khoáng với vai trò nhƣ các mầm apatite carbonate, đồng thời cũng là nguồn cung cấp ion calcium và ion phosphate cho quá trình phát triển mầm tinh thể và tinh thể apatite carbonate. Phân tích cấu trúc pha của hydrogel composit trƣớc và sau khi ngâm hydrogel composit trong dung dịch SBF bằng phƣơng pháp nhiễu xạ XRD khẳng định sự hình thành khoáng apatit của hydrogel composit sau khi ngâm trong dung dịch SBF. Giản đồ nhiễu xạ XRD của hydrogel và hydrogel composit trƣớc khi ngâm SBF [phụ lục 10] có các pic tinh thể Tóm tắt luận án tiến sĩ ngành khoa học vật liệu Trang 20 của PEG tại vị trí 9.10◦ và 23.30◦, và HAp 31,86 (2
File đính kèm:
 tom_tat_luan_an_nghien_cuu_tong_hop_vat_lieu_moi_trong_cay_g.pdf
tom_tat_luan_an_nghien_cuu_tong_hop_vat_lieu_moi_trong_cay_g.pdf

